《特殊医学用途配方食品注册管理办法》正式出台
□ 林雨晨 蒋炼娇 本刊记者

国医健食(北京)科技有限公司总经理 赵建军
在国家卫计委5月13日发布的《中国居民膳食指南(2016)》中,对特定人群的膳食营养做出了指南。该指南主要针对孕妇、乳母、2岁以下婴幼儿、2~6岁学龄前儿童、7~17岁儿童少年、老年和素食等特定人群的生理特点及营养需要,在一般人群膳食指南的基础上对其膳食选择提出特殊指导,表明了特定人群的膳食营养逐渐受到社会的关注。
随着各种政策法规的发布,作为特殊膳食用食品中的一部分—FSMP逐渐浮现在人们的视野中。中国政府高度重视特医食品的科学监管和规范发展,新颁布的《食品安全法》明确了特医食品的法律地位。为了贯彻落实新食安法,规范特医食品的监管工作,督促特医食品生产企业依法依规生产,国家食品药品监督管理总局颁布了《特殊医学用途配方食品注册管理办法》,于7月1日实施,使特医食品迎来了发展新机遇。
本文将从国内外特医食品政策法规发展情况、《特殊医学用途配方食品注册管理办法》简要解读与特医食品在国内的发展机遇这3方面进行介绍。
国内外特医食品政策法规发展情况
早期,在国际上的特殊医学用途配方食品从婴幼儿食品开始发展,是满足其生长发育需要,为各种先天代谢病患儿配置的特殊食品。首例特医食品产于1957年,经美国FDA批准作为孤儿药上市,用于苯丙酮尿症的膳食治疗。在1962年,美国FDA重新划分了医学营养的分类,将静脉注射医学营养品依旧保留在药物类别,经消化道肠胃吸收的营养品则归于特医食品分类。
1973年以前,所有的FSMP产品都是为婴幼儿制定的。直到1973年以后才出现了第一个成人全营养配方,1988年才有了第一个成人的疾病营养配方。随着成人疾病营养配方的问世,FDA将医学营养作独立分类,执行注册制。时间行至1996年,FDA进一步将特殊膳食补充剂和特殊医学营养品进行了区分,同时颁布了明确的产业政策。
目前,美国还延续着1988年FDA正式定义的“特殊医学用途配方食品”(Medical Foods)政策,包括了生产、抽样、检验和判定等多项内容,是对医用食品的生产和监管的指导原则。其对特医食品的定义为“用于特殊疾病或状态下的膳食管理,为满足特定营养需求,且基于公认的科学原则并建立在医学评估基础上的用于肠内的配方食物,其使用需要在医生的监护下进行”。
在欧盟,虽然有27个成员国,但是他们遵守着同一个特殊医学用途配方食品法规,法规将产品细分为1岁以下和1岁以上;1岁以上则遵循着3个分类,全营养标准配方食品、针对某种疾病或临床要求的全营养特定配方食品、非全营养标准配方或特定配方食品;其中,非全营养是单一蛋白质构成的兼膳,在欧盟指令中有规定成分标签的严格标示。
1989年,欧盟首次颁布了特殊营养目的用途食品标准,特医食品也被纳入其中进行管理,并在其1999年的增补条款中明确要求制定相应的FSMP标准。受欧盟委托,食品科学委员会(Scientific Committee of Food)于1996年完成了制定该标准的科学技术评估,特别是产品分类以及营养素限量的制定原则;1999年,欧盟正式颁布了FSMP标准。
在中国,特医食品从2009年立项至今已有近8年时间。在2010年,相关部门公布了《食品安全国家标准 特殊医学用途婴儿配方食品通则》(GB 25596-2010);2013年公布了《食品安全国家标准 特殊医学用途配方食品通则》(GB 29922-2013)、《食品安全国家标准 特殊医学用途配方食品良好生产规范》(GB 29923-2013)等食品安全国家标准;2014年正式颁布特殊医学用途配方食品的国标;2015年特殊医学用途配方食品列入新《食品安全法》;2016年3月《特殊医学用途配方食品注册管理办法》颁布,7月1日正式实施。由于我国特殊医学功能食品的普及率没有欧美及发达国家高,处于发展初期,对于政策的完善成为了推动特医食品市场发展的催化剂。
《特殊医学用途配方食品注册管理办法》简要解读
在中国,FSMP产品在法律层面得到进一步规范,《特殊医学用途配方食品注册管理办法》的制定可谓是特医食品发展的里程碑。
《特殊医学用途配方食品注册管理办法》(以下简称《办法》)按照依法严格注册、简化许可审批程序、产品注册与生产许可相衔接的思路和原则,主要规定了特医食品申请与注册条件和程序、产品研制要求、临床试验要求、标签和说明书要求,以及监督管理和法律责任等相关内容。《办法》明确特医食品是为了满足进食受限、消化吸收障碍、代谢紊乱或特定疾病状态人群对营养素或膳食的特殊需要,专门加工配制而成的配方食品;必须在医生或临床营养师指导下,单独食用或与其他食品配合食用。特医食品功效旨在改善病人营养状况,促进病人康复,缩短住院时间,节省医疗费等。
《办法》中具体内容包括8点,一是明确注册申请人的条件:该办法明确特医食品注册申请人应当为拟在我国境内生产并销售特医食品的生产企业和拟向我国境内出口特医食品的境外生产企业。二是明确注册申请的基本要求:该办法明确申请特医食品注册,应当向总局提交特医食品注册申请书、产品研发报告和产品配方设计及依据、生产工艺资料等8项材料,并对其真实性负责。三是明确现场核查与技术审查要求:该办法明确总局审评机构对申请材料进行审查,并根据实际需要组织对生产企业进行现场核查,对试验样品进行抽样检验和对临床试验进行现场核查。四是明确注册申请及批准时限要求:该办法明确核查机构应当自接到审评机构通知之日起20个工作日内完成现场核查,并出具核查报告。审评机构应当自收到受理材料之日起60个工作日内完成技术审评工作,并作出审查结论。食药总局应当自受理申请之日起20个工作日内对特医食品注册申请作出是否准予注册的决定。五是明确临床试验要求:该办法明确特定全营养配方食品需进行临床试验的,由申请人委托符合要求的临床试验机构出具临床试验报告。六是明确标签和说明书相关警示要求:特医食品的标签和说明书的内容应当一致,涉及特医食品注册证书内容的,应当与注册证书内容一致,并标明注册号。七是明确注销注册证书具体情形:该办法明确企业申请注销的、有效期届满未延续的、企业依法终止的、注册依法被撤销或撤回或注册证书依法被吊销的以及法律法规规定应当注销注册的其他情形,总局将依法办理特医食品注册的注销手续。八是明确相关违法行为的法律责任:该办法明确申请人隐瞒真实情况或者提供虚假材料申请注册的,不予受理或者不予注册,并给予警告;申请人在1年内不得再次申请。
特殊医学用途配方食品在中国的发展机遇
逐渐配备齐全的政策,为特殊医学用途配方食品在中国的发展铺就了必备的引导线,帮助企业在“规定的办法”中寻求机遇,在给企业带去收益的同时,建立品牌,保证优质、高效的产品,加大企业在市场中的占有率。同时,中国的实际国情与面临的社会问题,也促使特医食品能够在中国有长足发展。
中国人口众多,对此类产品的需求旺盛,特医食品在老年、儿童及孕妇等特殊人群的疾病治疗中提供营养支持及能起到显著改善作用。当前,全世界每年消费FSMP产品约560~640亿元,市场每年以6%的速度递增。欧美年消费量占据全球较大比重,约为400~500亿元,增速为4.5%;日本和韩国的市场规模为150~220亿元,增速为4.8%。澳大利亚每年在医用食品相关领域的消费数量超过4000万美元,新西兰的消费量约为250~400万美元。
数据显示,在亚洲,40%的住院病人都有发生营养不良的风险,1/3独立生活的老人也有营养不良的风险,低收入者、长期经受疼痛的病人营养不良风险很重。我国拥有13亿人口,但目前老龄化的问题越来越严重,加上生育率逐年降低,住院病人比例逐年攀高,社会经济收入贫富差距大等等问题都需要解决,在人民共同追求生活质量的当今,随着相关法规标准的逐步完善,中国特殊医学用途配方食品市场将迎来新的发展机遇。
针对上述机遇,本刊记者采访了国医健食(北京)科技有限公司总经理赵建军。国医健食是一家专业的特殊医学用途配方食品、保健食品的CRO公司。凭借对特医食品和保健食品、保健医疗器械行业长期的研究积累和服务经验,以及在这一过程中获取的政策法规、政府监管、产品准入、申请报批等方面的专业知识,国医健食为委托企业提供专业准入咨询等相关信息服务,帮助委托企业少走弯路,规避风险,提高成功率。在采访中,赵建军为我们介绍了特医食品在中国的发展前景和面临的问题。
记者:请您介绍一下国医健食(北京)科技有限公司及其专业合伙人团队,贵公司为特医行业的发展提供了怎样的业务帮助?
赵建军:国医健食是一家专业的特殊医学用途配方食品、保健食品的CRO公司。公司依托中国医药保健食品进出口商会强大的行业背景、可靠的专家资源和前沿的智力支持,专注于营养保健食品和特医食品的研发申报、临床研究、产业政策研究、产业数据挖掘、行业标准制定等业务,立足于做中国最好的营养保健产品和特医食品研发机构,把引领中国营养食品产业发展升级作为目标。
国医健食可以为特医行业提供咨询服务:产品的转让、项目论证、研发过程、生产过程、注册申报、人员培训、标准的制定、政策的解读、产品的营销策划等。
在组建国医健食合伙人团队的时候,我们要求成员必须是青年的一级一线专家。这种要求的原因是:我们首先要让国医健食的团队行走在科学的前沿;其次保证团队的战斗力和朝气。目前团队由1个海归专家、3个博士、2个硕士组成,分别从事药物和食品的研发、临床、注册等相关专业10年以上。团队曾与上海院士活动中心、中国中医科学院、北京中医药大学、北京协和医院、解放军301医院、四川大学华西医院等科学研究机构和上百家临床医院机构建立了长期稳定的合作关系。团队有服务于国药控股、河北石药、联邦制药、上海复星、永安药业、山东福胶、杭州味全、五粮液等国内知名企业的成功案例。
记者:据了解,早在上世纪8、90年代,特殊医学用途配方食品在欧洲、美国、加拿大等发达国家就得到了广泛的应用,是临床治疗中不可或缺的产品。您认为特医食品的作用是什么?请您对中国特医食品的发展背景作一下介绍。
赵建军:FSMP产品是为了满足进食受限、消化吸收障碍、代谢紊乱或特定疾病状态人群对营养素或膳食的特殊需要,专门加工配制而成的配方食品。
我们都知道,许多高消耗性疾病患者的死亡不是疾病直接导致的,而是由于营养不良、饥饿所导致。比如癌症病人,后期异常的消瘦;比如肾炎病人,由于疾病的原因不能过多摄入蛋白质,一方面没有合适的保证营养的食物,另一方面蛋白质摄入过量导致病情加重甚至死亡。特医食品就是病人的饭,它和我们知道的通过静脉注射的营养素不一样,是通过口服或管饲的方式来应用。当目标人群无法进食普通膳食或无法用日常膳食满足其营养需求时,特医食品可以作为一种营养补充途径,针对不同病症配备个性化方案,起到营养支持作用。
应当注意的是,此类食品不是药品也不是保健食品,不能替代药物的治疗作用,产品也不得声称对疾病的预防和治疗功能。国内特医食品市场被外国食品占据,长期以来依赖进口,处于量少价高的局面。这导致许多有需要的病人得不到合理的营养支持,给临床治疗带来了困难。
为满足国内市场对FSMP产品的需求,政府大力在我国发展特医食品,建立与国际接轨的相关配套的国家标准体系,2010年,原卫生部颁布《特殊医学用途婴儿配方食品通则》(GB 25596-2010),并于2013年第11号公告公布了《特殊医学用途配方食品通则》(GB 29922-2013)和《特殊医学用途配方食品良好生产规范》(GB 29923-2013)三项国家标准。
记者:请问特殊医学用途配方食品有哪些?
赵建军:从分类上来看,特医食品可按年龄段分两大类,即特殊医学用途婴儿配方食品(1岁以下)和特殊医学用途配方食品(1岁以上)。其中特殊医学用途配方食品(1岁以上)又分为3类:一是全营养配方食品,可当其作为长期单一营养来源时,能够满足目标人群的每天营养需求;二是特定全营养配方食品,这类食品针对脏器功能不全或衰竭、代谢障碍、机体对某营养素的需求增加或限制的特殊营养代谢状况的患者而设计,可当其作为单一营养来源不仅满足目标人群每天营养需要,而且能满足由于某种疾病和医学状况而产生的对某些营养素或日常食物特殊要求;三是非全营养配方食品,可以满足目标人群部分营养需要。
记者:您对于特医食品在中国的未来发展有何展望?
赵建军:特医食品在中国还是一个新兴事物,预测不敢说,但从目前现状来看,我认为有几点是可以肯定的。
第一,临床需求确实存在,目前虽然上述几大类特医食品大部分都存在于市场,但临床患者的需求并未真正得到满足,只是部分得到了满足,特别是在慢性病管理这块,缺口较大。第二,注册管理办法的出台和实施,标志着一个新领域的大门打开了。据国医健食了解,目前许多企业正在积极投身到这个领域中。有理由相信,未来市场上会出现更多的特医产品,并且由于本土企业的介入,无论是产品数量还是价格都将向有利于患者的方向发展。第三,特医食品要想得到更好的应用面临着几个需要解决的瓶颈问题。包括患者和医生的认知度偏低,观念的转变需要科学普及;费用较高,患者承受能力有限;专业人才队伍的缺乏等。特别是有关特殊医学食品的研究在我国还处于起步阶段,基础研究扎实、临床应用研究有据,能明确指导临床应用的产品很少。
在此,希望通过政府、企业、媒体、医院等社会各界的共同努力,推动FSMP产品在中国广泛使用,为患者提供营养支持,促进其健康的恢复。

相关热词搜索:
[责任编辑:]

 Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
 食品异物问题频发?是时候了解X射线检测了
食品异物问题频发?是时候了解X射线检测了
 开拓科技创新,撬动橡塑业高质量发展
开拓科技创新,撬动橡塑业高质量发展
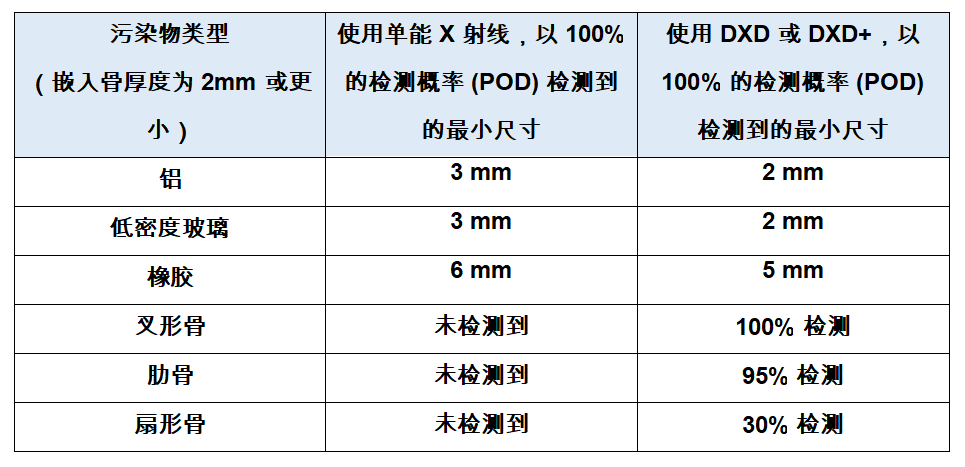 梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
 探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
 《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
 《保健食品真实世界研究通则》团标技术审查与特食跨
《保健食品真实世界研究通则》团标技术审查与特食跨
 凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
 精准把控 高质发展,第三届微生物安全与应用会议在
精准把控 高质发展,第三届微生物安全与应用会议在
 《食品行业科技创新白皮书》重磅发布!
《食品行业科技创新白皮书》重磅发布!






参与评论