关于美国“新膳食成分”备案指南的修订草案
□ 美中健康产品协会 供稿
对于美国膳食补充剂行业的许多企业而言,遵守1994年的膳食补充剂健康与教育法案(以下简称“DSHEA”),不仅复杂而且令人畏惧。因此,美国食品药品监督局(以下简称“FDA”)试图通过新膳食成分(以下简称“NDI”)法规的实施来整体改善质量措施的合规性。NDI备案指南的背景
1994年DSHEA法案生效时,市场上只有约4000个膳食补充剂产品。2012年的一份报告显示,FDA预计市面上的膳食补充剂数量增加到55600种,每年有5500多种新的膳食补充剂产品上市。而从1995年启动NDI备案工作至2014年12月,FDA仅受理完成750多个NDI备案。
随着越来越多的产品涌入市场,FDA一直努力在措施合理方面跟上脚步。为了让膳食补充剂更加安全,也为了减轻工作人员的负担,FDA发挥其权威性,在上市前的审批方面制定了更为清晰的法规。制药产业的新药审批或临床审批已经标准化,但是对于膳食补充剂产业而言,是一个巨大的挑战。
NDI的定义
新膳食成分是指1994年10月15日之前未在美国境内上市的膳食成分。根据美国联邦食品药品化妆品法案,膳食成分包括维生素、矿物质。因为其标准、定义和要求难以解释,所以,2016年8月,美国FDA在其官网发布了NDI备案指南修订草案,进行了为期60天的公开征求意见。该草案是2011年奥巴马签署FSMA后,FDA出台的第一版NDI备案指南的修订版。
根据美国联邦食品药品化妆品法案第413(a)(2)部分,生产商或经销商必须对即将使用的新膳食成分于上市前75天提交资料至FDA进行强制备案。需要注意的是,膳食成分必须是对人体产生一定影响的。如果添加入膳食补充剂的某种成分对人体没有任何作用,那么需要在使用前先获得审批,其中包括添加剂或染色剂,他们需要按照“一般认为安全(GRAS)”进行监管。
21 U.S.C. 321(ff)(1)(a)(b)(d)规定,维生素、矿物质和氨基酸可以是合成的;21 U.S.C. 321(ff)(1)(c)(f)规定,合成的草本植物成分不属于草本植物。其他特殊的定义和标准可查阅2011版美国联邦食品药品化妆品法案指南。
NDI备案的流程
任何在DSHEA法案后于美国上市的膳食补充剂都必须提交NDI备案申请,以便于FDA验证产品的安全性。制造商或分销商在申请NDI备案时需要提交以下资料:确认一种成分类别;关于判定该成分为NDI这一结论的论据;物理性质、化学或分子组成或成分结构的描述;供应商名单;原料和成分的规格(纯度、杂质或污染物的识别和等级);毒理研究获得的安全性数据包括NOAEL和NOEL;每日容许最大摄入量(ADI);怎样计算ADI;动物实验或人体实验(如果需要);生产流程。
NDI备案可以电子化提交,一旦提交了备案申请,FDA将在75天内给出回应。如果在此期间需要补充更多的信息或更新备案申请中的某些信息(例如更改生产流程),将重新按照75天进行计算。在FDA回应前,此膳食补充剂不可以分销或售卖。FDA会对NDI备案申请作出如下回应:无异议的确认信;不足以说明21CFR 190.6部分;存在安全性漏洞的拒绝信;根据21 U.S.C. 32l(ff)(1) or 21 U.S.C. 32l(ff)(2)存在监管问题。
NDI备案会在通过后90天进行公示,如果公司希望对其申请的NDI备案进行保密,需在提交申请期间告知FDA,FDA则不会将其公布在网站上。其他公司若想引用该NDI备案中的资料,必须得到持有者的书面授权。即使其他公司可以引用现有的NDI备案资料,也必须在申请中提交自己的数据和证据。

[责任编辑:]

相关阅读
- (2015-03-31)美国食品包装中针对抗菌剂的法规概述
- (2017-03-14)美国食品安全现代化法案下的食品出口
- (2017-11-20)美国FDA食品生产现场检查要点解读
- (2014-06-27)《中华人民共和国食品安全法(修订草案)》的新亮点(二)
- (2014-09-03)食品安全法修改草案有关条款的修改建议
 Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
 食品异物问题频发?是时候了解X射线检测了
食品异物问题频发?是时候了解X射线检测了
 开拓科技创新,撬动橡塑业高质量发展
开拓科技创新,撬动橡塑业高质量发展
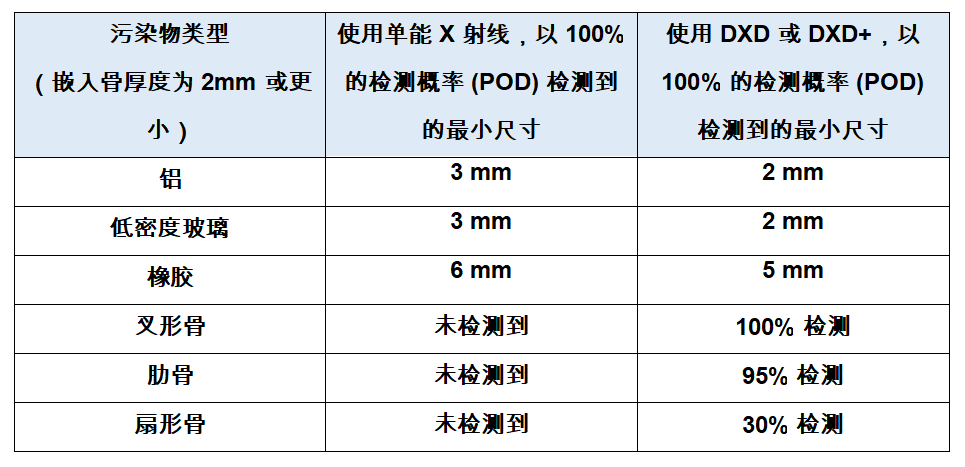 梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
 探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
 《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
 《保健食品真实世界研究通则》团标技术审查与特食跨
《保健食品真实世界研究通则》团标技术审查与特食跨
 凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
 精准把控 高质发展,第三届微生物安全与应用会议在
精准把控 高质发展,第三届微生物安全与应用会议在
 《食品行业科技创新白皮书》重磅发布!
《食品行业科技创新白皮书》重磅发布!






参与评论