转谷氨酰胺酶交联对 大豆分离蛋白乳化性的影响研究
摘要:本论文通过转谷胺酰胺酶交联大豆分离蛋白,并对交联后大豆分离蛋白溶解乳化性和乳化稳定性的变化进行了研究。实验结果表明交联前乳化性为15.86m2/g,交联后乳化性为13.23m2/g,经转谷氨酰胺酶交联后乳化性有所降低,降低了16.6%。乳化稳定性交联前为38.2min,交联后为60.8min,交联后乳化性稳定性显著提高,提高了37.2%。
关键词:转谷氨酰胺酶;大豆分离蛋白;乳化性
转谷氨酰胺酶(TGase)是一种能催化蛋白质中赖氨酸上的Ɛ-氨基与谷氨酸上ɤ-羟酰胺基之间发生联合反应的酶。此酶能聚合蛋白多肽之间形成共价聚合物。天然的未经加工的大豆分离蛋白(SPI)的功能尚不能满足人们在日常生产中的需求。为避免传统方法对改性SPI的副作用,SPI经过酶的改性处理进一步广泛地应用于食品及其他工业中。SPI乳化性在食品工业应用广泛,SPI作为乳化剂可使产品达到较理想的稳定状态。目前已大量应用在诸多产品的生产中。乳化性大小在很大程度上取决于外界压力水平、压力处理时间及溶剂性质[1]。SPI的结构及与其他物质的交互作用也对SPI的乳化性影响较大[2]。SPI的乳化性与二硫键含量呈负相关。本试验对TGase交联SPI乳化性和乳化稳定性变化进行了研究。
材料与方法
材料。大豆吉农:34由吉林农业大学生命科学学院提供 ;转谷氨酰胺酶购于sigma公司
方法。(1)乳化性及乳化稳定性的测定:采用Pearce and Kinsella 方法[3]测定乳化性(EAI))和乳化稳定性(ESI)。用磷酸盐缓冲溶液(10mmol/L,pH7.0)配制成1%酶交联前后的SPI溶液。加入大豆油,按照250m了/L的比例。均质10min,在1000r/min条件下,把溶液均质成均一的乳化液。分别取0min和10min的乳化液1mL,用0.1%的十二烷基磺酸钠(SDS)稀释至10mL,立即用分光光度计,以0.1%的SDS为空白,测得500nm的吸光度值。乳化性=2×2.303A0×N/10000R×L×C,乳化稳定性= A10t/(A0- A10)
其中A0为0min时的吸光度值,A10为10min时的吸光度值,t为两次测定的吸光度值时间间隔10min,L为比色杯厚度,R为油相体积,C为蛋白质浓度,N为稀释倍数。
结果与讨论
TGase对大豆分离蛋白乳化性和乳化稳定性的影响。蛋白质的乳化性能可以由乳化活力和乳化稳定性来表征。本研究用TGase交联前后EAI和ESI的变化来表示酶交联对蛋白质乳化性能的影响。交联前乳化性为15.86m2/g,交联后乳化性为13.23m2/g,经TGase交联后乳化性有所降低。乳化稳定性交联前为38.2min,交联后为60.8min,交联后乳化性稳定性显著提高。可能与交联后表面疏水性、二硫键的含量变化有关[4]。
讨论。本试验对最佳条件下,交联SPI溶解性、乳化性和乳化稳定性变化进行了研究。经TGase交联后SPI溶解性和乳化性均下降,乳化稳定性增加。本研究结果与田少君等[5]的研究结果相一致。
结论
通过对TGase交联后SPI功能特性研究结果表明,交联后,溶解性下降了7.4%,乳化性降低了16.6%,乳化稳定性增加了37.2%。
参考文献
[1]Diftis N, Kiosseoglou V. Improvement of emulsifying properties of soybean protein isolate by conjugation with carboxymethyl cellulose[J]. Food Chemistry, 2003, 81(1):1-6.
[2]杨锋,刘雪,任仙娥,等.不同商用大豆分离蛋白结构特征和功能性质的比较[J] .现代食品科技,2016,09:107-115.
[3] Wang X S,Tang C H, B S,et al. Effects of high-rressure treatment on some physicochemical and functional properties of soy protein isolates [J].Food Hydrocolloids, 2008, 22(4):560-567.
[4]Effect of cryopreservation on surface hydrophobicity and disulfide bonds of soybean protein isolate liquid dispersion[J].Food Science, 2014, 35(7):28-32.
[5]田少君,梁华民.转谷氨酰胺酶对大豆分离蛋白的改性研究[J] .粮油加工与食品机械,2005,(06):54-56.
臧学丽
长春医学高等专科学校

相关热词搜索:
[责任编辑:]

 Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
Mettler-Toledo 在中国国际渔业博览会上展示创新的产品
 食品异物问题频发?是时候了解X射线检测了
食品异物问题频发?是时候了解X射线检测了
 开拓科技创新,撬动橡塑业高质量发展
开拓科技创新,撬动橡塑业高质量发展
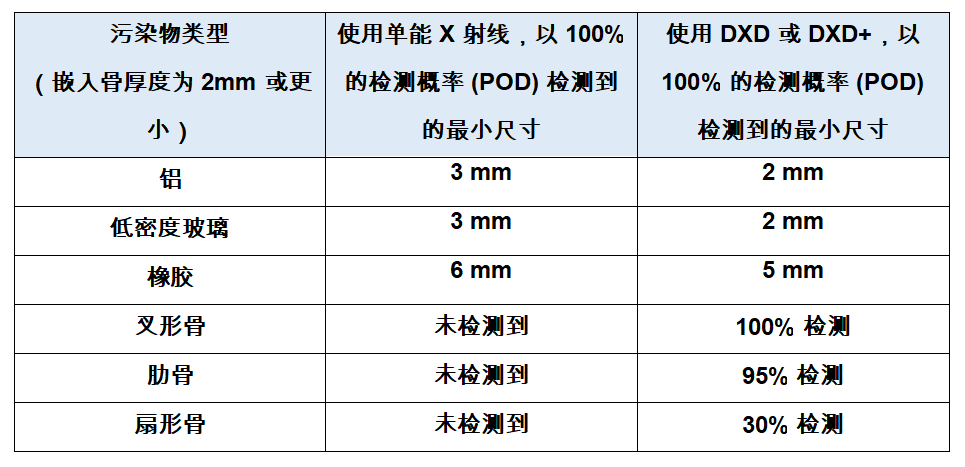 梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
梅特勒托利多针对“难以发现”的污染物推出高品质X射线检
 探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
探索婴幼儿辅食市场高质量发展之路,为宝宝成长保驾护航
 《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
《食品安全最佳实践白皮书(2021-2022年)》四大主题发布
 《保健食品真实世界研究通则》团标技术审查与特食跨
《保健食品真实世界研究通则》团标技术审查与特食跨
 凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
凝聚全球食饮智慧 SIAL西雅展国际化水平再创新高
 精准把控 高质发展,第三届微生物安全与应用会议在
精准把控 高质发展,第三届微生物安全与应用会议在
 《食品行业科技创新白皮书》重磅发布!
《食品行业科技创新白皮书》重磅发布!






参与评论