食品中的致病微生物沙门氏菌的商业化检测技术
□ 贺丽丽 拜发分析系统销售(北京)有限公司
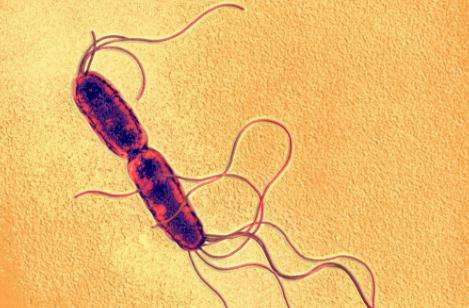
沙门氏菌是食品中常见的致病菌,也是引起食物中毒的重要病原菌之一,其会严重危害人们的食品安全与身体健康。据统计,在全球记载的细菌性食物中毒事件中,因沙门氏菌而引起的食物中毒常列榜首。
沙门氏菌疾病是公共卫生学上具有重要意义的人畜共患病之一,其病原菌——沙门氏菌属肠道细菌科,包含多种能引起食物中毒及导致胃肠炎、伤寒和副伤寒的细菌。沙门氏菌在粪便、土壤、食品和水中可存活5个月至2年之久,除可感染人体外,其还可感染哺乳类、鸟类、爬行类、鱼类、两栖类及昆虫等动物。人/畜感染沙门氏菌后可呈现无症状带菌状态,也可表现为有临床症状的致死疾病——加重病态或提高死亡率,亦或降低动物的繁殖能力。
家禽、蛋类和肉类产品是沙门氏菌的主要传播媒介,而受感染程度主要取决于沙门氏菌的血清类型和食用者的身体状况,因此,小孩、老年人及免疫缺陷的个体是较容易受到该菌威胁的群体。根据国际惯例,要求对易受沙门氏菌污染的食品进行检测,并分类管理,以保证消费者接触到的食物不含沙门氏菌,从而有效预防疾病。我国《食品安全法》规定,食品中沙门氏菌的限量标准为0,并要求食品在进入市场之前一定要检测是否含有沙门氏菌。然而,传统的细菌学检测方法繁琐耗时,不能满足如今食品安全检测快速发展的需求。本文介绍了德国拜发集团(以下简称“拜发”)在食品中沙门氏菌检测方面研发的3种检测方法,以期为相关人员进行日常检测提供参考。
1 实时荧光PCR方法(RT-PCR)
1.1 应用原理
RT-PCR(Real time-PCR)是在传统PCR反应体系中加入荧光基团,利用荧光信号的积累实时检测整个PCR进程,最后通过软件分析其积累的荧光信号,进而对需要检测的基因序列进行定性或定量分析。
拜发研制的用于沙门氏菌检测的荧光定量检测试剂盒SureFast® Salmonella ONE可进行100次扩增。该试剂盒包括样品提取和扩增两部分,用户只需对所要检测的样品进行约20小时的简单预增菌,然后全部使用试剂盒所提供的耗材及试剂进行实验,最终只需不到2小时便可得到准确的定性结果。
1.2 具体操作流程
实时荧光PCR方法(RT-PCR)的样品提取及检测流程如下:
①根据《说明书》的指示,取500μL预培养的培养液,加入500μL裂解液,95℃孵育10分钟后放置于常温环境中1分钟。然后,将其清液作为样品液进行扩增。
②进行扩增缓冲液的配置,加入样品后放入RT-PCR仪器中进行扩增,约1小时就可根据软件中的信号收集分析样品结果。该试剂盒的结果包括阳性质控、阴性质控、过程质控及内部抑制质控(IAC)等。
1.3 检测优势
由于PCR具有高灵敏性,易因污染或特异性差等原因产生假阳性结果,而通过阳性质控、阴性质控、过程质控的结果,检测人员可以快速判定试剂盒是否有效,是否出现假阳性结果。但是,如因样品自身或环境中存在抑制剂等情况而造成所有的结果均为阴性,又应如何判定该阴性结果是因为试剂失效,还是环境因素,亦或样品因素,从而出现假阴性的判定结果呢?常见的沙门氏菌抑制剂有EDTA、血红蛋白、铁乳蛋白、肝素、胆盐、蛋白酶类、胆红素、腐植酸、富里酸等,它们在血液、粪便、食品和环境中都会出现,从而导致整个实验失败。
在荧光定量检测试剂盒SureFast® Salmonella ONE中,根据ISO 22174:2005的要求,拜发在进行每个样品扩增实验的同时,还会要求用户做内部抑制质控(试剂盒内包含所用到的全部试剂)。这样,在判定样品是否为阴性时,实验条件为内部抑制质控阳性、阴性样品,过程质控阴性、阳性质控阳性,只有这4个条件同时达到才能认为所检测的样本为阴性。
为了验证荧光定量检测试剂盒SureFast® Salmonella ONE的准确性、灵敏度及稳定性等相关参数,拜发团队使其参与了AOAC-RI及MicroVal(ISO 16140-2)的验证工作,并顺利通过。该试剂盒使用过程非常简单,不需要专业的微生物检测人员进行操作,其检测目标物为沙门氏菌的目标DNA,检测结果真实可信,不需要再次进行确证实验。同其它的沙门氏菌检测方法及成熟的商业化检测试剂相比,该方法是较快的确证方法,可以指导工厂筛选原料、清理环境、降低库存压力,从而减少对专业技术人员的依赖,节省劳动力。在沙门氏菌的检测中,其不失为一种适用于大型工厂指导生产的有效工具。
2 酶联免疫吸附技术(ELISA)
2.1 应用原理
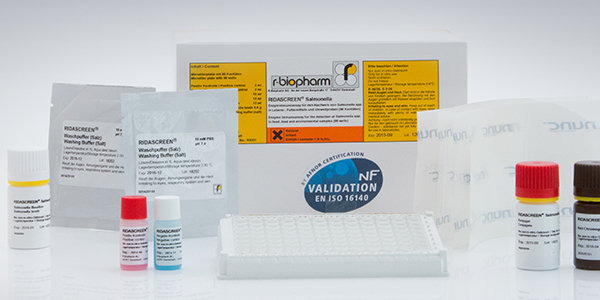
RIDASCREEN® Salmonella沙门氏菌检测试剂盒R4201可用于经隔夜预增菌后的样品中运动性和非运动性沙门氏菌(包括S.pullorum和S.gallinarum)的检测。该检测中使用“一步预增菌法”用以复苏和活化受损的沙门氏菌,并令其继续繁殖——微孔板上包被的特异性纯化沙门氏菌抗体可选择性地捕获样品中的沙门氏菌;被捕获的沙门氏菌将在添加了试剂盒中所含的增菌培养基微孔板内继续繁殖;随后,将孔内的增菌培养基转移到新的微孔中,通过在原微孔板中加入沙门氏菌抗体酶结合物使夹心酶联反应法得以继续;没有结合的酶结合物被洗去,再向孔内加入色原/显色剂,在酶的作用下将其转化为蓝色产物;加入反应终止液,使蓝色的孔内反应液颜色变黄。若孔内反应液呈现无色,则表示样品预增菌汤,即被检样品为沙门氏菌阴性。

2.2具体操作流程
①RIDASCREEN® Salmonella预增菌(隔夜):将25g(mL)样品(或取样菌种)加入到225mL缓冲蛋白水中,在35~37℃条件下孵育16~20小时。
②检测准备过程:沙门氏菌板内增菌培养基在50mL无菌蒸馏水中溶解,于100℃中加热10分钟,使用前回温至35~37℃。洗涤缓冲液在1L无菌蒸馏水中溶解,使用前预热至35~37℃。
③捕获样品中的沙门氏菌:滴加质控和经预增菌后的样品各100μL放入反应微孔板中,于35~37℃下孵育30分钟(孵育时请盖住反应微孔板)。
④第一次清洗:重复清洗7次,每次每个微孔各对应使用300μL洗涤缓冲液(预热至35~37℃)。
⑤受损菌的营养增菌:在各反应微孔中滴加250μL沙门氏菌,板内增菌培养基于35~37℃下孵育4小时(孵育时请盖住反应微孔板)。
⑥样品转移/预留被检样品:将经板内增菌的沙门氏菌菌汤全部转移到新的微孔中,保留其用于检测阳性结果的确认和鉴定。
⑦加入酶连接物:在各反应微孔中滴加入100μL酶连接物,于35~37℃下孵育30分钟(孵育时请盖住反应微孔板)。
⑧二次清洗:重复清洗7次,每次每个微孔各对应使用300μL洗涤缓冲液(预热至35~37℃)。
⑨加入色原/显色剂,目测结果:在各反应孔中加入100μL色原/显色剂,室温下暗室孵育15分钟,若孔中反应液呈蓝色,则表示被检样品为沙门氏菌阳性。
⑩终止反应,使用仪器测量和分析检测结果:在各反应孔中加入100μL反应终止液,于450/620nm波长下使用合适的仪器进行结果测量,根据《说明书》进行结果判定。
2.3检测优势
作为初筛样品中是否含有沙门氏菌的检测方法,ELISA法具有明显的检测优势:检测总时长不超过24小时;样品处理简单;不需要大型仪器,利用普通的酶标仪即可初步判断样品是否为疑似样品;同样,其也不需要专业的技术人员进行操作,且样品基质适应范围广,可以检测食品、饲料、环境等各种样品。RIDASCREEN® Salmonella沙门氏菌检测试剂盒R4201灵敏度高,25g样品中只需含有1~5个沙门氏菌即可检出;检测通量大,经过简单的样品处理,一次可以检测近90个样本。该试剂盒通过了法国农业部AFNOR的认证(RBP31/01-06/08),其检测结果同相关标准方法接近或相似,可信度高。
3 传统的微生物培养法
3.1 应用原理
Compact Dry SL沙门氏菌检测板是一种干燥培养基产品,含有显色底物和新生霉素,其可通过运用以下3个独立的测试原理来检测样品中的沙门氏菌:
①沙门氏菌的赖氨酸脱羧酶使培养基碱性化(培养基颜色将由蓝紫色变为黄色);
②沙门氏菌特有的酶会使显色底物裂解,从而形成绿化的菌落(沙门氏菌产生硫化氢会形成黑色菌落);
③沙门氏菌的运动性。
3.2 具体操作流程
①根据食品安全国家标准GB 4789.4-2016《食品微生物学检验 沙门氏菌检验》5.1的要求或拜发产品HS9401用法说明对样本进行约20小时的预增菌后,再根据ISO 6579:2002进行约24小时的增菌,然后根据HS 9401用法说明中的第三、第四步骤将增菌后的培养基置于Compact的平板上,在42℃环境下孵育24小时后判定结果。
②根据《说明书》,当出现黑色-绿色的菌落时,意味着此样品中可能含有沙门氏菌。为确证这一想法,此时可以移取检测板上的黑色-绿色菌落并根据相关标准进行下一步的沙门氏菌生化鉴定。
3.3 检测优势
该方法共需约3天时间就可以初步判定结果;成本低廉,无需制备培养基和压片;简单易操作,一般技术人员都可熟练掌握。此外,检测板上的菌落清晰易测,可将单个菌落分离出来进行鉴定实验,类似于目前的国标方法。
4 总结
以上3种产品均为拜发自主研发并生产,如用户无时间方面的压力,可以选择同传统国标方法相似的沙门氏菌微生物培养法进行检测;如果用户生产时间紧迫,库存压力大,且在仪器方法的操作方面不够成熟,建议选择ELISA方法尽快完成对原料的初筛及对成品的初步判定,让完全阴性的原料可以尽快生产或让完全阴性的成品尽快进入市场;如果用户自身仪器配套设施较为完备,则建议选择第三种方法进行定性检测,其速度快,不需要再次进行选择性培养及血清学筛查,且节省劳动力,过程简单,使用的耗材处理简单、安全,不会轻易对环境及人员造成污染,不失为一种实验室检测沙门氏菌的优选方法。

相关热词搜索:
[责任编辑:]

 挪帝克开设京东旗舰店 与京东全球购达成战略合作
挪帝克开设京东旗舰店 与京东全球购达成战略合作
 2019《食品安全导刊》杂志订阅返百元红包!
2019《食品安全导刊》杂志订阅返百元红包!
 9月大事 | 市场监管总局开展2018年全国“质量月”活动
9月大事 | 市场监管总局开展2018年全国“质量月”活动
 盒装水果省事不卫生 实验解释3大疑问
盒装水果省事不卫生 实验解释3大疑问
 “食安中国网”手机站上线通知
“食安中国网”手机站上线通知
 食安中国网关于2015年春节放假的通知
食安中国网关于2015年春节放假的通知
 第十三届中国国际食品安全与质量控制会议(2019CIFSQ)
第十三届中国国际食品安全与质量控制会议(2019CIFSQ)
 食品安全 快乐参与 百元礼品 免费获取食品
食品安全 快乐参与 百元礼品 免费获取食品
 企业交流学习的桥梁 食品人技能提升的平台
企业交流学习的桥梁 食品人技能提升的平台
 探讨食品安全未来趋势 引领食品安全技术发展
探讨食品安全未来趋势 引领食品安全技术发展
 CAC (China) HACCP内审员
CAC (China) HACCP内审员





参与评论