白及清肺养胃口服液质量标准研究
□ 王勇 张志勇 贵州省食品药品检验所
□ 张炯怡 宋晓宁 李松 李静锋 贵州省食品检验检测院
摘 要:为建立白及口服液的质量标准,本研究采用TLC法对白及清肺养胃口服液中的白及进行定性鉴别,采用紫外-可见分光光度法测定多糖含量。结果显示,TLC鉴别中供试品与白及和酸浆对照药材在相应位置上显示相同的颜色斑点。3批供试品中,多糖平均含量不少于1.5%。故得出结论,采用水提醇沉法制备口服液具有效率高、适合大规模生产等特点。该质量控制方法快速、准确,可有效控制白及清肺养胃口服液的质量。
关键词:白及口服液 薄层色谱 多糖 质量标准
白及为兰科白芨属植物,英文名为Bletillae Rhizoma,拉丁种名为Bletilla striata (Thunb.) Reichb.f.,主产于贵州、四川、浙江、湖南等省份,为多年生草本植物。《中国药典》2020版一部指出,白及具有收敛止血、消肿生肌等功效[1]。《本草汇言》论述“白及敛气,止血,消痈之要药也。此药极粘腻,痈肿可消,溃败可托,有托旧生新之妙用也。”由此可见,白及既有助于止血消痈,还具有封填破损、托旧生新的组织修复功能。白及的用药历史悠久,应用广泛,药效显著,目前已分离出联苄类、菲类、黄酮类、苯丙素类、甾体、三萜等成分[2]。此外,白及是传统止血生肌的重要药材,临床用于消化道溃疡和出血的效果显著。现代研究表明,白及多糖是白及中的主要有效成分——可通过黏附作用在胃黏膜表面形成一层保护膜,起到保护和修复溃疡面的作用[3]。巩子汉[4-6]等研究表明,白及多糖可通过下调PI3K及Akt mRNA和蛋白表达水平来抑制细胞因子IL-2R及IL-4的异常分泌,通过下调JNK 及P38 MAPK基因和蛋白表达水平来抑制炎症因子TNF-α、IL-1β及IL-6的异常分泌;通过下调模型大鼠血清IL-2R、上调IL-4含量和胃组织Caspase-8表达而发挥保护胃黏膜的作用。除此之外,白及还具有其他多种药理作用,如抗菌、抗胃溃疡、抗氧化等[7-11]。本课题组以传统中医药理论为指导,按照保健食品的配方要求,研制出白及清肺养胃口服液,并以《保健食品行政许可受理审查要点》中保健食品质量标准的相关要求对本品进行质量标准研究,旨在为白及相关产品的开发提供基础依据。
1 仪器与材料
1.1 仪器
Linomat-5半自动点样仪、REPROSTAR 3薄层色谱成像系统(CAMAG);GZX-9030MBE型电热恒温古风干燥箱;超纯水机;薄层层析硅胶G板,青岛海洋化工厂;UV-2401PC紫外可见分光光度计,日本岛津;AE-240型电子天平,梅特勒-托利多仪器(上海)有限公司;DFD 700数显恒温水浴锅;Mettler AE-240型电子天平,梅特勒-托利多仪器(上海)有限公司。
1.2 材料
白及对照药材,批号:AF20021021;乙腈(色谱纯),国药集团化学试剂有限公司;蒽酮、硫酸、甲醇、无水乙醇等,均为分析纯;白及口服液,实验室自制;D-无水葡萄糖对照品;水为屈臣氏纯净水。
2 方法与结果
2.1 性状
本品为口服液,内容物为黄褐色粘稠液体。
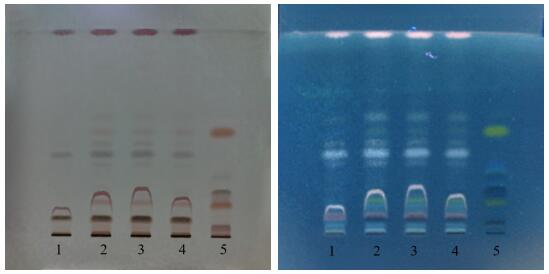
图 1 白及的 TLC 鉴别
(注:1 为缺白及阴性样品、2~4 为 3 批供试品、5 为白及对照药材。)
2.2 薄层鉴别
鉴别①为制剂中白及药材的薄层色谱鉴别。取样品醇沉,过滤,滤液蒸发至近干,加水复溶,乙酸乙酯萃取,乙酸乙酯层作为供试品溶液。取白及对照药材用70%乙醇超声提取后照供试品制备方法制备对照药材溶液,另取不含白及药材的阴性制剂作为阴性对照溶液。分别吸取上述溶液点涂于薄层层析硅胶G板上,使其呈条带状,分别以甲醇-乙酸乙酯-环己烷(1.5︰2.5︰6)、甲苯-甲醇(5︰1)、甲苯-甲醇(9︰1)、甲苯-乙酸乙酯(9︰1)为展开剂展开,取出并晾干,以10%的硫酸乙醇溶液作为显色剂向板上喷洒,加热(105℃)至斑点清晰。结果显示,以甲苯-乙酸乙酯(9︰1)为展开剂的展开分离效果较好,阴性对照无干扰,结果见图1。
鉴别②为制剂中酸浆药材的薄层色谱鉴别。试验考察了制剂未萃取和萃取后采用二氯甲烷和乙酸乙酯萃取的薄层色谱鉴别效果,发现采用乙酸乙酯萃取后样品的展开效果良好,故选择乙酸乙酯萃取,并取乙酸乙酯层作为供试品溶液。阴性对照溶液以不含酸浆药材的阴性制剂同法制备,对照药材溶液以酸浆药材加甲醇超声提取制备。分别吸取上述溶液点涂于薄层层析硅胶G板上,使其呈条带状,分别以甲醇-乙酸乙酯-环己烷(1.5︰2.5︰6)、三氯甲烷-丙酮-甲醇(25︰1︰1)、甲苯-甲醇(5︰1)、甲苯-乙酸乙酯(9︰1)为展开剂展开,取出并晾干,以10%的硫酸乙醇溶液作为显色剂向板上喷洒,加热(105℃)至斑点清晰。结果显示,以甲苯-乙酸乙酯(9︰1)为展开剂的展开色谱斑点分离好,显色清晰,阴性对照无干扰,结果见图2。
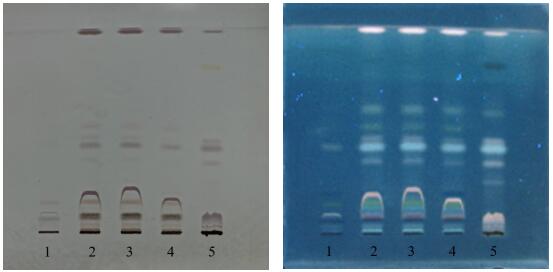
图 2 酸浆的 TLC 鉴别
(注:1 为缺酸浆阴性样品、2~4 为 3 批供试品、5 为酸浆药材。)
2.3 重金属检查
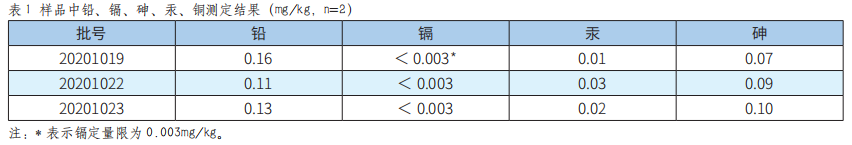
参照《食品安全国家标准 食品中铅的测定》(GB 5009.12-2017)第一法:石墨炉原子吸收光谱法、《食品安全国家标准 食品中镉的测定》(GB 5009.15-2014)、《食品安全国家标准 食品中总砷及无机砷的测定》(GB 5009.11-2014)第一篇第二法:氢化物发生原子荧光法、《食品安全国家标准 食品中总汞及有机汞的测定》(GB 5009.17-2014)第一篇第二法:冷原子吸收光谱法对样品中铅、镉、总砷、总汞的含量进行测定,结果见表1。
2.4 多糖含量测定
现代研究表明,白及含有多类小分子化合物,但含量均较低,并不适合作为控制白及质量的指标。白及多糖作为白及的主要活性成分,含量高达20%,具有促进造血、止血、治疗口腔溃疡与胃溃疡、增加免疫因子的表达、愈合烫伤创面、抗菌和抗肿瘤等作用。本品为白及与酸浆果实的水提物,含有一定量的多糖,通过白及药材化学成分的研究从中制备出白及多糖,并以其为指标成分控制白及及制品的质量。
2.4.1 供试品溶液的制备
精密称取本样品2g置于50mL容量瓶中,加水溶解并稀释至刻度,摇匀,离心,取上清液5mL,加无水乙醇30mL,摇匀,静置1h,离心5min(4000r/min),弃去上清液,沉淀热水溶解后用量筒定容至50mL,摇匀,即得。
2.4.2 对照品溶液的制备
精密称取干燥至恒重的18.09mg D-无水葡萄糖对照品置于100mL量瓶中,加水溶解并稀释至刻度,制成每1mL含0.1809mg无水葡萄糖的对照品储备液。
2.4.3 蒽酮硫酸试液的配制
精密称取蒽酮0.2g置于100mL容量瓶,加硫酸溶解并稀释至刻度,摇匀,即得。
2.4.4 测定波长的选择
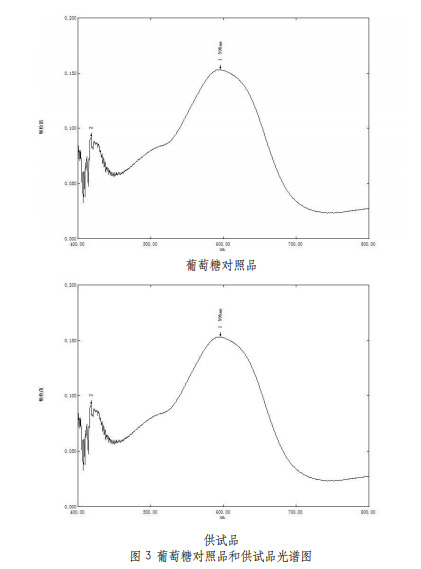
分别精密量取1mL供试品和D-无水葡萄糖对照品溶液置于不同刻度管中(10mL),分别加入1.0mL水,摇匀,再分别加入0.2%蒽酮硫酸溶液各6mL,混匀,沸水浴放置10min后立即冰浴冷却10min,取出后以相应试剂为空白对照,测量光谱图,对照品和供试品在波长590nm处均有最大吸收,见图3。
2.4.5 标准曲线的制备
精密量取对照品储备液0.2、0.4、0.6、0.8、1.0mL置于10mL刻度管中,加水至2.0mL,摇匀,加入0.2%蒽酮硫酸溶液6mL,混匀,沸水浴中加热10min后立即冰浴冷却10min,取出后以相应试剂为空白对照,在625nm处测定吸光度,以吸光度A为纵坐标,质量数(mg)X为横坐标,绘制标准曲线(见图4),并计算回归方程与相关系数。回归方程为A=4.4002X +0.0014(r=0.9996),线性范围为0.0362~0.181mg。
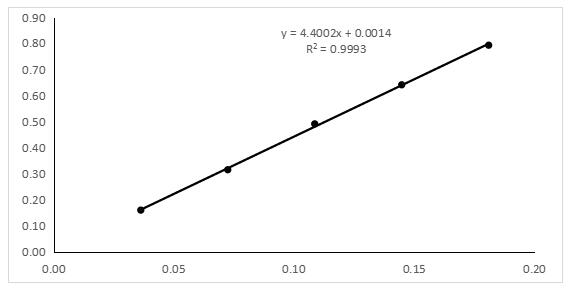
图 4 工作曲线图
2.4.6 重复性试验
精密称取样品1.0、2.0、3.0g各3份,按供试品溶液制备方法制备供试液,精密量取供试液2mL,按标准曲线制备项下的方法——精密加入0.2%蒽酮硫酸溶液6mL,依法测定吸光度。结果显示,供试品在1~3g的称量范围内,方法重复性良好。
2.4.7 对照品溶液和供试品溶液显色后稳定性考察
分别取葡萄糖对照品1mL和供试品2mL,加水至2.0mL,用0.2%蒽酮硫酸溶液显色,以相应的试剂作空白对照,测定吸光度,每隔10min读数,共考察50min。结果显示,对照品溶液和供试品溶液的吸光度平均值分别为0.507、0.332,RSD分别为0.43%、0.16%,表明本法测定样品显色后在50min内稳定。

2.4.8 准确度
2.4.8.1 精制白及多糖的提取和精制
称取50g白及药材粗粉,回流提取2h(80%乙醇),共提取2次,弃去提取液;继续用热水提取残渣2次,浓缩提取液,加入一定量乙醇,使醇含量达到80%,静置醇沉,沉淀物加水溶解后用Savage法除蛋白5次,再醇沉第二次;分别用无水乙醇和丙酮洗涤沉淀物,挥去有机溶剂,即得精制白及多糖。
2.4.8.2 换算因子的测定
精密称取21.60mg白及多糖置于100mL容量瓶中,加水定容至刻度,再精密量取5mL该溶液置于10mL量瓶中,加水至刻度,定容,摇匀,即得多糖供试品溶液。然后,精密量取1mL供试品溶液测定吸光度。以多糖质量数与无水葡萄糖质量数的比值为换算因子f,即f=W/C。通过测量计算,换算因子平均值为f=1.718,RSD值为1.39%,见表2。
2.4.9 回收率
称取精制白及多糖304.93mg置于50mL量瓶中,加适量热水溶解,放冷,用水稀释至刻度,摇匀,得到每1mL含白及多糖6.0986mg的溶液。精密称取1g已测定多糖含量的制剂(平均含量以无水葡萄糖计为1.82%,换算为多糖再计算回收率)置于50mL量瓶中,共称取9份,分别精密加入白及多糖溶液2.5、5、7.5mL,每个体积3份(所取样品量中多糖质量数的50%、100%和150%),供试品溶液的制备方法同上。结果显示,本法平均回收率为100.4%,RSD为2.8%。
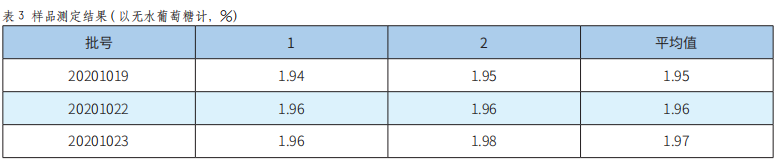
2.4.10 制剂中多糖含量的测定
按质量标准草案制备供试液和对照品溶液,用0.2%蒽酮硫酸溶液显色,测定3批样品中多糖的含量,结果见表3。
根据制备工艺研究和含量测定结果,暂定本品含多糖以无水葡萄糖计,不得少于1.5%。
参考文献:
[1] 国家药典委员会.中华人民共和国药典:一部[S].2015年版. 北京:中国医药科技出版社,2015:103.
[2] 刘金梅,安兰兰,刘刚,刘育辰.白及化学成分和药理作用研究进展与质量标志物预测分析[J/OL].中华中医药学,2018:1-22.
[3] 程安媛.新型胃粘附材料-白芨多糖的制备及膜粘附性体内外评价.中国优秀硕士学位论文全文数据库,2008,01.
[4] 巩子汉,王强,段永强,等.白及多糖对胃溃疡模型大鼠胃组织TNF-α、IL-1β、IL-6及JNK、p38 MAPK基因蛋白表达水平的影响*[J].中药药理与临床,2019, 35(4):90-94.
[5] 巩子汉,虎峻瑞,段永强,等.白及多糖对胃溃疡模型大鼠血清IL-2R、IL-4及胃组织Caspase-8水平的影响[J].中国中医药信息杂志,2019,26(10):35-39.
[6] 巩子汉,王艳威,段永强,等.白芨多糖对GU模型大鼠胃组织PI3K/Akt的影响[J].中国实验方剂学杂志,2020,26(6):52-57.
[7] 吕小波,黄春球,武正才,等.白及多糖对胃溃疡大鼠防治作用的实验研究[J].云南中医学院学报,2012,35(1):30-32+45.
[8] 彭芙,万峰,熊亮,等.白及不同提取部位抗耐甲氧西林金黄色葡萄球菌的体内外活性[J].中国实验方剂学杂志,2013,19(17):217-220.
[9] 吕迪,李伟平,潘平,等.白及块茎和须根抑菌作用的研究[J].中国实验方剂学杂志,2013,19(5):212-216.
[10] 孔令姗.白芨多糖的提取与功效研究[D].上海应用技术学院,2015.
[11] 黄进,李娅,邱丽莎,等.不同干燥方法对白及花营养成分和抗氧化活性的影响[J].中国医院药学杂志,2017,37(19):1942-1946.
基金项目:贵州省科技厅科技支撑项目(黔科合[2016]支撑2856)。
作者简介:王勇(1985-),男,博士,副高,主要从事植物化学和药物分析研究。

相关热词搜索:
[责任编辑:]

 挪帝克开设京东旗舰店 与京东全球购达成战略合作
挪帝克开设京东旗舰店 与京东全球购达成战略合作
 2019《食品安全导刊》杂志订阅返百元红包!
2019《食品安全导刊》杂志订阅返百元红包!
 9月大事 | 市场监管总局开展2018年全国“质量月”活动
9月大事 | 市场监管总局开展2018年全国“质量月”活动
 盒装水果省事不卫生 实验解释3大疑问
盒装水果省事不卫生 实验解释3大疑问
 “食安中国网”手机站上线通知
“食安中国网”手机站上线通知
 食安中国网关于2015年春节放假的通知
食安中国网关于2015年春节放假的通知
 食品掺假与成分检测网络研讨会
食品掺假与成分检测网络研讨会
 权威专家解读食品中的丙烯酰胺及含量控制措施,快来
权威专家解读食品中的丙烯酰胺及含量控制措施,快来
 专家齐聚第三届全球食品安全共治论坛,启动食品安全
专家齐聚第三届全球食品安全共治论坛,启动食品安全
 中国国际食品安全与质量控制会议
中国国际食品安全与质量控制会议
 全球食品安全创新平台第四期入围项目名单揭晓,37个
全球食品安全创新平台第四期入围项目名单揭晓,37个






参与评论